在临床肿瘤学中使用人源化小鼠的研究在提高转化潜力方面已经取得了实质性进展,而原位肿瘤能更好地模拟肿瘤细胞在机体内生长的微环境,有更强的抗肿瘤免疫反应。科伴生物凭借其独特的脐带血资源和自主研发的huHSC-NOG-EXL小鼠原位瘤模型,提供高性价比的免疫人源化小鼠原位瘤模型,为抗肿瘤免疫创新药的研发提供了可及性高、临床转化性强的肿瘤模型。
科伴huHSC-NOG-EXL小鼠原位瘤模型特点
■ huHSC-NOG-EXL免疫人源化小鼠较PBMC人源化小鼠模型呈现了更完整的人的免疫系统;
■ 在huHSC-NOG-EXL免疫人源化小鼠体内构建的原位PDX/CDX肿瘤模型更接近人类肿瘤的特征;
■ 在huHSC-NOG-EXL免疫人源化原位肿瘤小鼠模型上获得的药效学结果具有更高的临床转化性;
■ 独特的脐带血资源和自主研发的huHSC-NOG-EXL小鼠原位瘤模型,可以提供高性价比的免疫人源化小鼠原位瘤模型;
利用人CD34+ HSPCs植入免疫缺陷小鼠产生了人免疫系统的小鼠,其具有比PBMC人源化的小鼠更完整的造血系统,包括先天免疫细胞、适应性免疫细胞和少量红细胞和血小板。将CD34+ HSPCs移植到SCID小鼠中产生了先天性和适应性的细胞谱系。但是植入的模型仍有一定的局限性,所以在CD34+ HSPCs植入后,在免疫缺陷小鼠中引入了许多改进基因,以增强人类免疫系统的发育和功能。我们自主研发的NOG-EXL 小鼠是新一代 NOG 小鼠衍生品系,是在 NOG 小鼠基础上引入编码人类 IL-3 和 GM-CSF 的转基因小鼠, 与基础 NOG/NSG 小鼠相比,huHSC 移植后,人源的单核细胞、树突状细胞和其他重要的细胞类型均有大幅增加, 呈现了更完整的人类免疫系统。NOG 小鼠具备超重度免疫缺陷特性(T、B、NK 细胞缺失),补体活性降低,巨噬细胞和树突状细胞功能失调,携带 NOD 背景中特异性 Sirpa 等位基因,这些特性使其成为人的免疫系统移植的优质宿主。huHSC-NOG-EXL 人源化小鼠中髓系细胞表达上升,呈现了更完整的人的免疫系统,为肿瘤免疫治疗的临床前研究提供了较好的体内研究平台,极大地促进及改善了肿瘤免疫疗法的研发进程。
huHSC-NOG-EXL特点
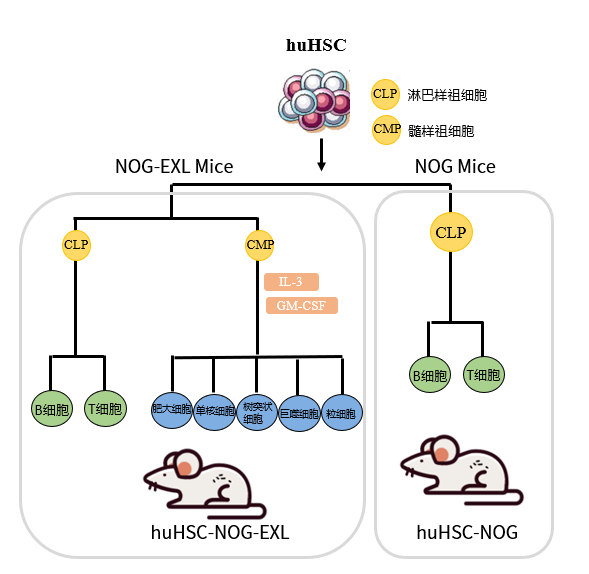
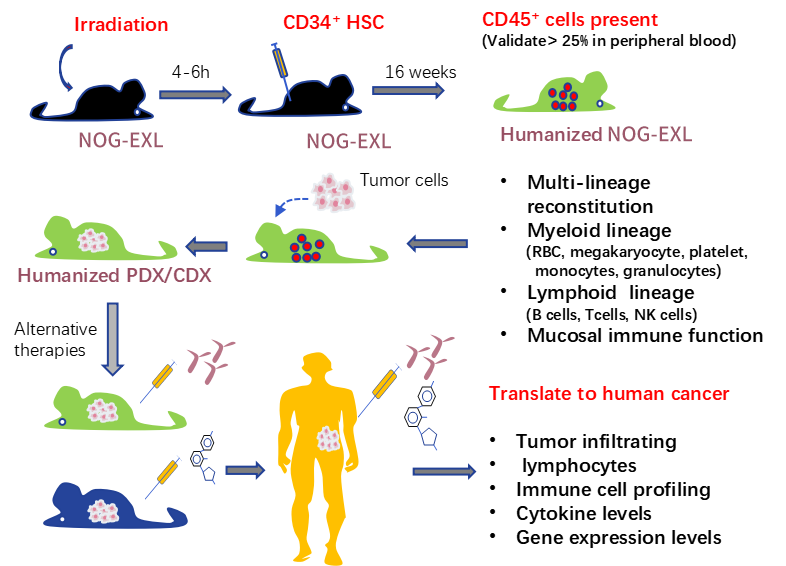
模型构建流程
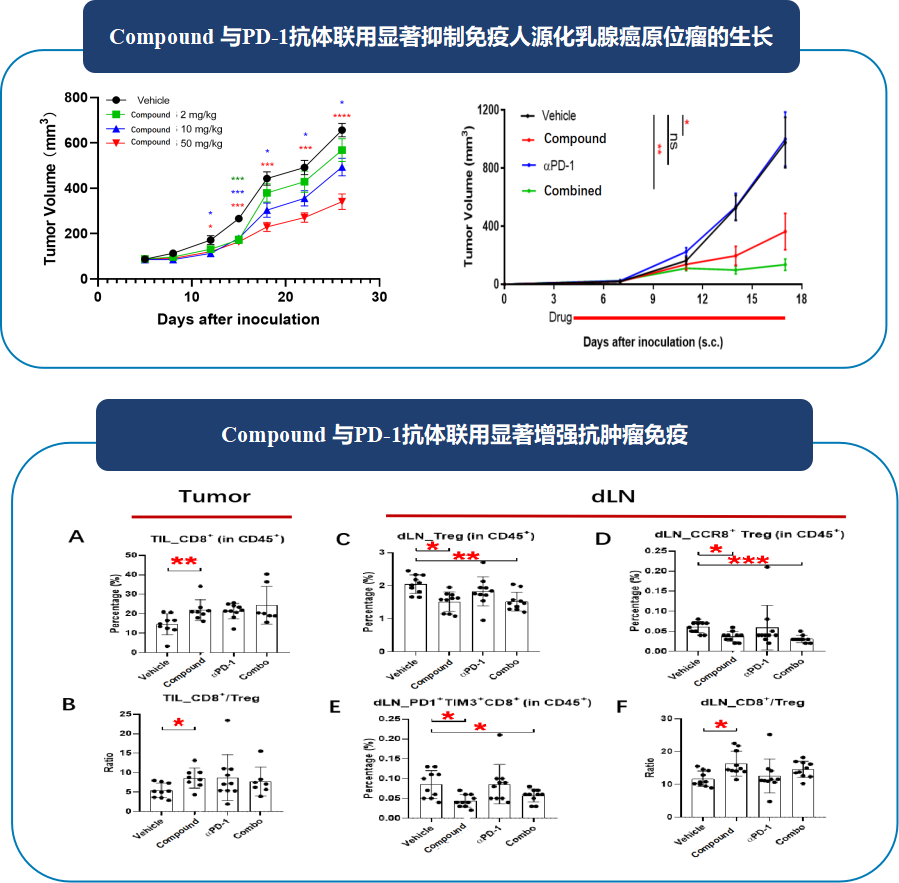
药效机制研究






Copyright © 2023 科伴生物科技(合肥)有限公司 All rights reserved 皖ICP备2023012129号